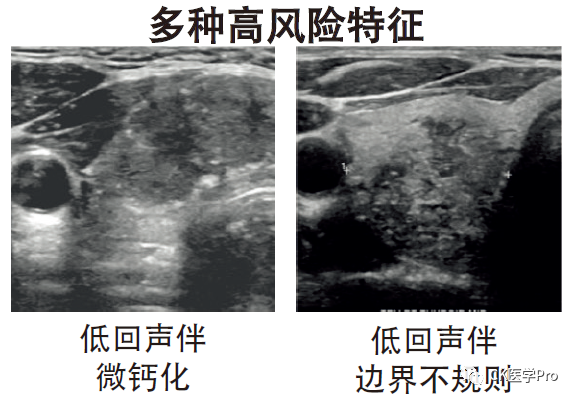
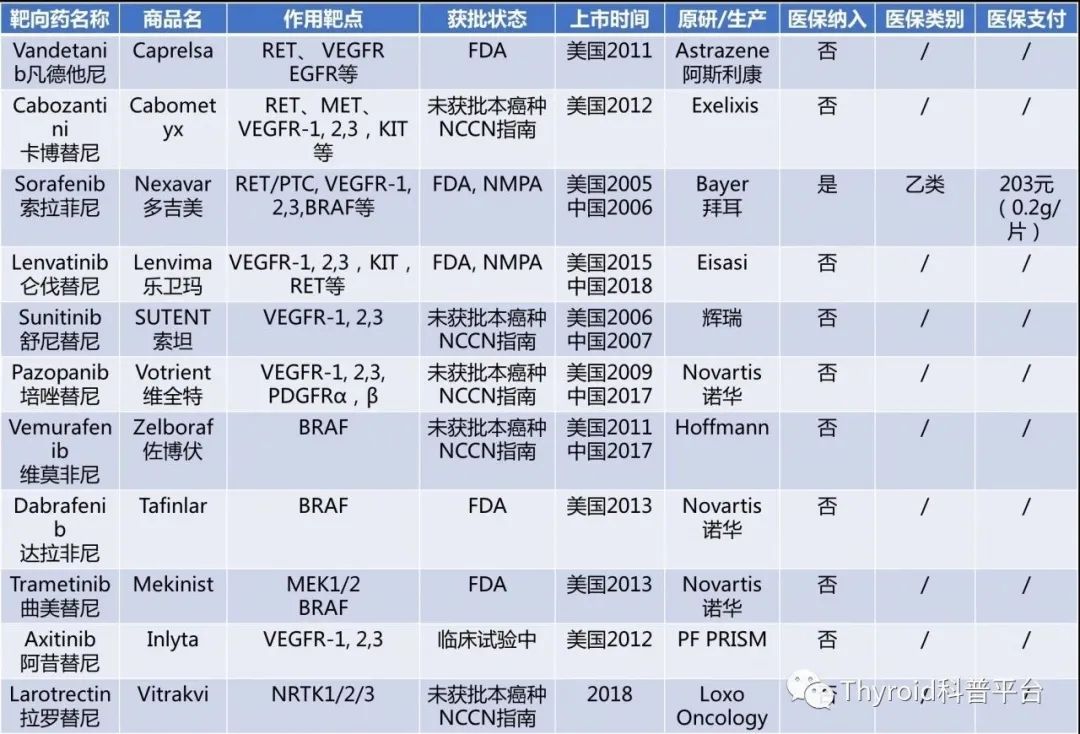
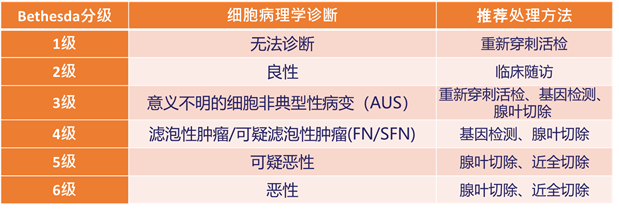
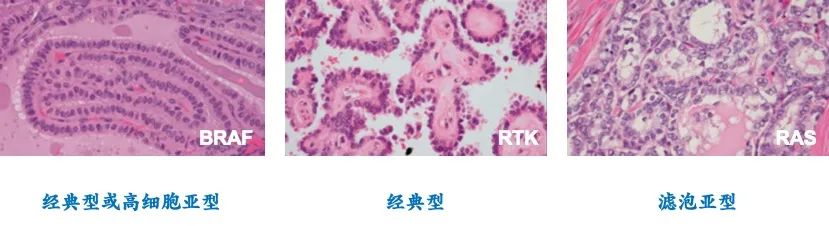
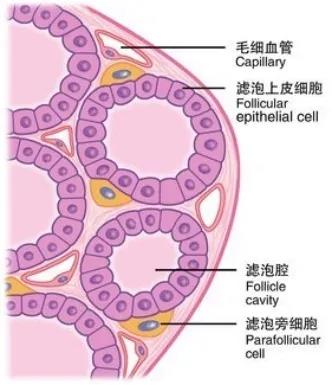
甲状腺的患友们常常有类似的问题。 甲状腺癌是最常见的内分泌系统恶性肿瘤,在过去的30年里,甲状腺癌的检出率提高了近3倍。 尽管这些肿瘤通常生长缓慢,且手术结合甲状腺激素抑制和/或放射性碘很容易进行针对治疗; 然而,一些患者也有可能进展成更具侵袭性和致命性的甲状腺癌,如低分化或未分化甲状腺癌。 目前针对甲状腺癌的基因检测主要包括BRAF, RAS, TERT突变以及RET/PTC1, PET/PTC3, PAX8/PPAR gamma基因重排等。 2014年《细胞》杂志上的一篇研究分析了近500个甲状腺癌样本,并鉴定出相应的遗传学突变,发现了一些新的癌基因以及现有基因的一些新变异。 如下图所示: BRAF基因位于7q34染色体上,和肿瘤细胞的生长、分化和凋亡等密切相关。 BRAF基因突变后,其活性比BRAF没有突变的提高上百倍,导致细胞异常增殖和分化。 目前发现的与人类肿瘤相关的BRAF基因突变约65种,其中BRAFV600E (T1799A点突变) 最为常见,高发于甲状腺癌和恶性黑色素瘤,也见于结直肠癌、卵巢癌、乳腺癌和肺癌。 1.提高诊断准确性: 甲状腺结节的细针穿刺细胞学检查(FNA)是当今评估甲状腺结节最可靠的手段,具有创伤小,准确率高等优点; 然而,仍有20-30%的甲状腺结节无法通过FNA明确诊断。 此类患者如果检测到BRAFV600E基因突变,那么高度怀疑为甲状腺癌。 2.影响手术方案制定: 确诊为甲状腺癌后,需要接受规范的治疗。 如果治疗前就检测到BRAFV600E突变,提示肿瘤侵袭性比较强,可能合并多个病灶,在手术方案的选择上,倾向于更大范围的手术方案。 3.参与碘-131治疗前评估: BRAFV600E基因突变已被纳入病人复发危险度分层的考量范围内,如:当1-4cm的局限于甲状腺内的甲状腺乳头状癌(PTC),同时伴BRAFV600E突变时,此类患者被纳入中危组;PTC伴BRAFV600E基因与TERT基因同时突变时,被纳入高危组。 核医学科医师将参考复发危险度分层信息,同时结合实时评估结果综合判定是否需进行碘-131治疗,及对碘-131治疗的目标及获益进行决策。 4.影响预后: 若甲状腺癌术后检测到BRAFV600E基因突变,提示该肿瘤相比于BRAF没有突变的肿瘤具有更高的复发转移率。 这类患者需要适当缩短随访的间隔期。 因此,BRAF基因突变的检测对甲状腺癌的诊断、治疗和判断预后都有重要的意义。 针对BRAF突变的靶向药物有哪些? 研究显示,伴有BRAF基因突变的患者其转移灶往往摄取碘-131的能力变差,导致碘-131不能聚集其中发挥其应有的杀伤肿瘤细胞作用。 其中部分病人被称为:碘难治性甲状腺癌,此类病人往往还合并TERT基因突变,患者的转移灶摄碘能力明显受损,使碘-131无法到达病灶呈碘难治性。 还有一种情况,病灶仍摄取碘但肿瘤大小或甲状腺球蛋白水平仍呈增长趋势。 此类患者总体预后显著降低。 针对上述病人现在可以通过给予患者服用针对BRAF突变的靶向药物,使部分病灶恢复对碘-131的摄取,进而提高碘治疗效果,使病灶得到有效的控制,这也从另一方面验证了BRAF基因突变对碘-131治疗效果的影响作用。 下图列出了目前已经批准或者正在进行临床试验的甲状腺癌靶向药物。 其中,索拉非尼、维莫非尼、达拉非尼、曲美替尼等都可以靶向抑制BRAF基因突变。 可见,针对BRAF基因突变我们并非无计可施。 BRAFV600E基因突变对于甲状腺癌是一种重要的诊断标记物和治疗靶点,可以指导医师选择最佳的治疗方案。 同时,也可以作为一个潜在的预后因子为甲状腺癌的随访方案制定提供依据。 参考文献 Cancer Genome Atlas Research Network. Integrated Genomic Characterization of Papillary Thyroid Carcinoma. Cell. 2014 Oct 23;159(3):676-90. Guerra A, Di Crescenzo V, Garzi A, Cinelli M, Carlomagno C, Pepe S, Zeppa P, Tonacchera M, Vitale M. Diagnostic utility of BRAF V600E mutation testing in thyroid nodules in elderly patients. BMC Surg. 2013;13 Suppl 2:S37. Zhu X, Luo Y, Bai Q, Lu Y, Lu Y, Wu L, Zhou X. Specific immunohistochemical detection of the BRAF V600E mutation in primary and metastatic papillary thyroid carcinoma. Exp Mol Pathol. 2016 Feb;100(1):236-41. Park KS, Oh YL, Ki CS, Kim JW. Evaluation of the Real-Q BRAF V600E detection assay in fine-needle aspiration samples of thyroid nodules. J Mol Diagn. 2015 Jul;17(4):431-7. BRAFV600E Mutation Associated With Non-Radioiodine-Avid Status in Distant Metastatic Papillary Thyroid Carcinoma.Clin Nucl Med. 2014 Aug;39(8):675-9. Cheng W, Liu R, Zhu G, etc.Robust Thyroid Gene Expression and Radioiodine Uptake Induced by Simultaneous Suppression of BRAF V600E and Histone Deacetylase in Thyroid Cancer Cells. J Clin Endocrinol Metab. 2016 Mar;101(3):962-71. Liu J, Liu R, Shen X, etc. The Genetic Duet of BRAF V600E and TERT Promoter Mutations Robustly Predicts Loss of Radioiodine Avidity in Recurrent Papillary Thyroid Cancer. J Nucl Med. 2020 Feb;61(2):177-182. Yang X, Li J, Li X, etc. TERT Promoter Mutation Predicts Radioiodine-Refractory Character in Distant Metastatic Differentiated Thyroid Cancer. J Nucl Med. 2017 Feb ;58(2):258-265. 作 者 : 侯 鹏 西安交通大学第一附属医院 审校专家: 林岩松 北京协和医院 王卓颖 上海交通大学医学院附属仁济医院甲状腺癌有哪些基因学改变?

什么是BRAF基因突变?
检测BRAF突变有什么临床意义?